Категории
- Советы
- Технологии
- Часто задаваемые вопросы
- Тесты
- Емкость мАч
- Номинальная вместимость
- сравнение
- everActive
- Аккумуляторы и аккумуляторы
- Накопленная энергия
- Долговечность аккумуляторных батарей
- Эффективность аккумуляторных батарей
- Напряжение аккумулятора
- ЛР03 ААА
- ЛР6 АА
- ENELOOP
- АГ13 ЛР1154 ЛР44
- ЧР 2032
- Дельта V
- Циклы зарядки
- внутреннее сопротивление
- Уровень заряда
- Эффект памяти
- Аккредитованный тест
- СР44 357
- Слуховые батарейки 675
- СР626 377
- Батарейки для часов
- Полярность
- Мач
- пассивация
- ЛС 14250
- ЛС 14500
Как работает аккумулятор?
2019-06-19
Глядя на аккумулятор, мы видим, что у него два полюса - один положительный, помеченный "+", другой отрицательный - отмеченный "-". В случае типичных цилиндрических батареек, таких как R6/AA или R14/C (используемых, например, для питания фонарей или игрушек), клеммы являются концами батареи. В автомобильных аккумуляторах полюса представляют собой тяжелые свинцовые клеммы.
Электроны накапливаются на отрицательном полюсе аккумулятора. Если соединить отрицательную и положительную клеммы проводом, то электроны будут двигаться как можно быстрее от отрицательной к положительной - батарея очень быстро разрядится (кроме того, мы не советуем проводить такого рода эксперименты из-за связанных с ними опасностей - никогда не замыкайте батарейку таким образом "на короткое время"!). В обычных условиях мы подключаем груз к аккумулятору с помощью кабеля – лампочки, мотора или электронной схемы, например, магнитолы.
Внутри батареи происходит реакция, в результате которой образуются свободные электроны. Скорость, с которой электроны высвобождаются в результате этой реакции (внутреннее сопротивление - сопротивление - батареи), очевидно, ограничивает количество электронов, которые могут протекать между полюсами. Электроны должны течь от батареи по проводу и нагрузке, от отрицательной к положительной клемме, чтобы произошла химическая реакция, которая высвободит еще больше их электронов. По этой причине мы можем оставить батарею неиспользованной на полке, например, на год, а затем продолжать использовать ее без каких-либо проблем - пока электроны не перетекают с отрицательной на положительную клемму, химическая реакция не происходит. В момент соединения полюсов – начинается реакция.
Химические реакции в аккумуляторах
Одним из самых простых аккумуляторов является цинк-углеродный аккумулятор. Глядя на реакции, происходящие внутри него, мы можем легче понять общий принцип работы всех батареек. Представьте, что у нас есть банка с серной кислотой (H2SO4). Если поместить в него цинковый стержень, то коррозийная кислота сразу же начнет его растворять. Мы увидим, как пузырьки водорода собираются на поверхности цинка, и стержень, и кислота начнут нагреваться.Вот что происходит:
- молекулы кислоты распадаются на три иона: два иона H+ и один ион SO4
- Атомы цинка на поверхности стержня теряют два электрона (2e-) и превращаются в ионы Zn++
- Ионы Zn++ соединяются с ионами SO4-- с образованием ZnSO4, который растворяется в кислоте
- электроны из атомов цинка соединяются с ионами H+ и образуют молекулы H2 (газообразный водород)
- Электроны начнут двигаться по проволоке и соединяться с водородом на углеродном стержне, из которого теперь также начнут развиваться пузырьки водорода
- значительно снизится тепловыделение; Используя электричество, протекающее по проводу, мы можем, например, запитать лампочку и измерить результирующее напряжение и ток, протекающие по проводу - часть тепловой энергии преобразуется в движение электронов.
Аккумуляторы, которые мы знаем, работают по тому же принципу. Они различаются по типам металлов и используемых электролитов, но все они работают благодаря одному и тому же явлению – электроны перетекают от одного полюса к другому. В зависимости от используемых компонентов меняется и характеристическое напряжение такой батареи. Давайте рассмотрим пример типичного свинцового автомобильного аккумулятора:
- Батарея содержит одну пластину из свинца и другую из диоксида свинца, обе погружены в электролит высококонцентрированной серной кислоты
- свинец соединяется с SO4 с образованием PbSO4 и одного свободного электрона
- диоксид свинца, ионы водорода и ионы SO4, а также электроны со свинцовой пластины образуют PbSO4, а воду на пластине – из диоксида свинца со временем две пластины покрываются PbSO4, и вода смешивается с кислотой; характеристическое напряжение составляет около 2В - так, соединив 6 элементов последовательно, мы получаем батарею ячеек с напряжением 12В
- цинк-углеродные аккумуляторы – настолько популярны, что их иногда называют «обычными»; являются наиболее часто используемыми батареями таких размеров, как R6/AA, R14/C, R20/D; электроды изготовлены из цинка и
- углерод, между которыми зажата кислотная паста, служащая электролитом
- Аккумуляторы А
Соединение элемента/батареи
В предыдущих рассуждениях мы использовали слова «батарея» и «элемент» как взаимозаменяемые. Это согласуется с тенденцией, преобладающей в повседневном языке. Однако с технической точки зрения слова «батарея» и «элемент» имеют совершенно разные значения. Таким образом, «элемент» означает один источник питания, например, такой как банка с кислотой, описанная в начале, и два стержня, соединенных проводом (или, например, «палец» R6/AA). «Аккумулятор» — это набор соединенных элементов (например, аккумулятор 3R12, состоящий из трех элементов в одном корпусе, соединенных последовательно). Именно в этом смысле мы будем использовать эти два термина в следующей части настоящего текста.В большинстве устройств мы, как правило, не используем одну клетку. Вместо этого мы подключаем несколько из них – либо последовательно, для большего напряжения, либо параллельно, для более высоких токов. При последовательном соединении получаем сумму напряжений подключенных ячеек; при параллельном подключении - сумма токов, полученных от составляющих ячеек.
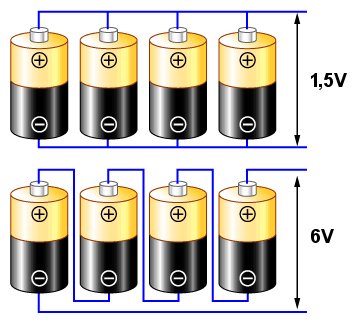
Соединение, как на верхней схеме, называется параллельным. Если предположить, что каждая ячейка имеет характерное напряжение 1,5 В (как типичная одиночная цинк-углеродная или щелочная ячейка), то напряжение, полученное на торцевых клеммах (обозначено стрелками), все равно будет составлять 1,5 В, но полученный ток будет в четыре раза выше, чем полученный от одной ячейки.
Соединение, как на нижней схеме, называется последовательным. В этом случае напряжения от отдельных ячеек суммируются, давая напряжение 6 В между клеммами.
При покупке аккумулятора или элемента обычно можно прочитать на упаковке, какое у него напряжение – иногда еще и емкость. Например, типичные аккумуляторные батареи, используемые в цифровых камерах, имеют напряжение 1,2 В и емкость 2000 мАч. Емкость в 2000мАч (мАч – это аббревиатура от миллиампер-час) означает, что, теоретически, такая батарея способна обеспечить ток в 2000мА (2000 миллиампер, т.е. 2 ампера) в течение часа, ток в 1А в течение двух часов, ток в 100мА в течение 20 часов и т.д. Однако клетки обычно ведут себя не так линейно. Во-первых, каждая батарея имеет максимальный ток, который она способна выдавать. Таким образом, батарея емкостью 500 мАч не сможет обеспечить 30 А тока в течение секунды, потому что химические реакции, происходящие внутри батареи, никак не могут обеспечить такое количество электронов за такое короткое время. Во-вторых, при сильном токе элементы обычно сильно нагреваются, что приводит к потере большого количества их энергии. В-третьих, многие химические системы, используемые в батареях, служат короче (или дольше!) при очень низком энергопотреблении. Тем не менее, емкость, измеренная в ампер-часах, дает хорошее представление о том, как долго данная ячейка прослужит при определенном потреблении тока при типичных условиях эксплуатации.
Авторское право Baltrade ©
Добавить комментарий